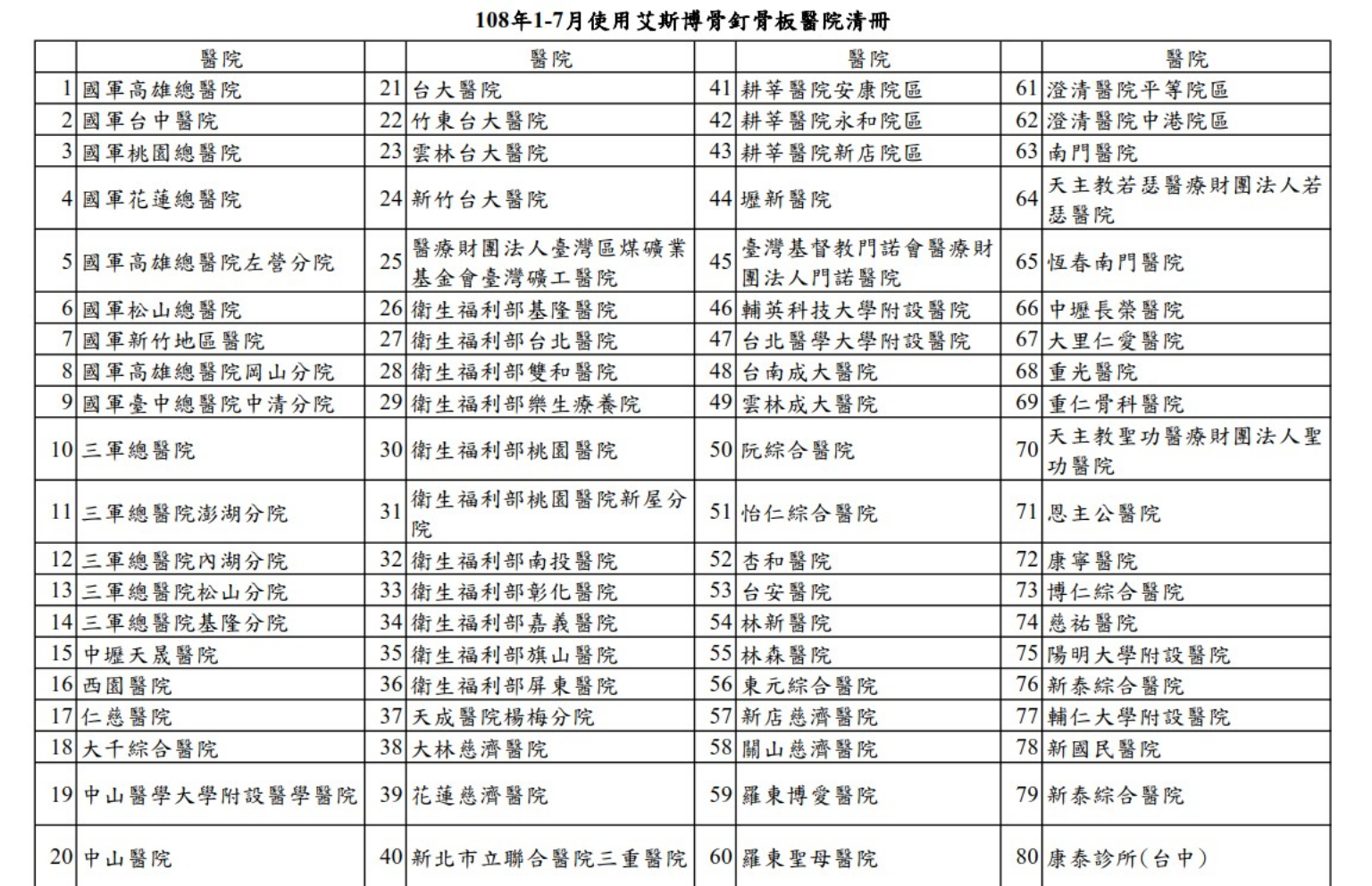
日前傳出「喜維克骨釘骨板系統」廠商艾斯博有限公司(下稱艾斯博),委託仕成精密科技股份有限公司,在尚未取得GMP認證前,擅自製造並供應7萬多支鈦合金骨釘骨板流入200多家院所,食藥署已於日前要求艾斯博立即啟動產品回收,並宣布共有80家醫院疑似用到違法產品,台大、三總、中山、花蓮慈濟、衛福部醫院都上榜。
食藥署品質監督管理組副組長遲蘭慧表示,針對在尚未取得GMP認證就擅自製造骨釘、骨板的業者,食藥署已要求艾斯博公司立即啟動回收作業,目前也已接獲艾斯博公司繳交回收報告,共計回收75,299支骨釘、骨板,並由高雄市政府衛生局協助清點,仍有部分數量尚待釐清。
「為確認回收作業確實完成,食藥署已於10月8日派各地方衛生局至轄內醫療院所確認庫存狀況,案內產品於各醫療院所均已無庫存。」遲蘭慧表示。
這個骨釘骨板的醫材特性如何?為什麼民眾願意自費高達4-7萬元不等的鈦合金骨科醫材?病人裝了沒有GMP認證的醫材會出現什麼問題?如何避免類似的事再發生?
80家醫院受害...換委託商為何醫院不知情?
「它是一種鎖定骨板,這種骨板的固定性比較牢靠,針對一些關節附近、粉碎型或是骨質疏鬆的骨折患者,它的特別塑性裝置會讓患者的癒合恢復比較快又穩定。」新光醫院骨科主任釋高上,接受《信傳媒》電訪時先解釋。
釋高上指出,艾斯博是一間國產廠牌,其「喜維克骨釘骨板系統」大概使用5年內。「艾斯博以前委託的廠商有獲得GMP的認證,但是後來中間有轉移廠商,就沒有GMP的執照,推斷可能是新找的這家廠商在還未GMP認證時就先製造了。」
那醫院對於這樣沒有GMP認證的廠商是否知情?
釋高上認為醫院一般是不知情的,「因為原本一直都是使用同一家廠商,醫院只認廠商,但廠商委託誰製造,醫院可能就不會去深究這部分。我知道有些醫院像台大其實會深究,但這次廠商沒有告知換了委託廠商,所以台大也疏忽掉了。」他表示,許多外國廠牌只要一換生產點就會立刻告知,醫院也會重新審核。
這次新光醫院沒有在受害的醫院榜上,釋高上表示,「我們沒有使用這家廠商、主要都是用國外的,也不是說國外比較好,重點還是要確認有沒有獲得GMP認證,這方面還是要謹慎一點。所以在醫材審核這部分醫院也要更仔細,連委託商、上游部分都要注意,才能避免之後類似的事情發生。」

病人裝非法骨科醫材,會有哪些影響?
那是否有病人裝了這個骨釘骨板後出現問題?
釋高上表示目前沒有特別聽聞,不過他強調,「廠商有沒有GMP認證,就代表製造過程是否優良,如果沒有被認證,品質的穩定度很難掌控,也不是說這個骨板一定會有什麼危害,但它就是沒有被認證。就像今天沒有被認證的藥廠產出的藥,聲稱有療效,民眾也會不能相信。」
他表示過去也曾碰過較極端的例子,是中國製造的骨板,「再拔起來的時候發現它生鏽了,代表品管出現問題。因為一個骨板要放在身體裡面,不能說擺久就腐蝕掉、或是強度就改變,所以這個東西的品質就格外重要才需要認證。」
不過釋高上也認為,因為骨板畢竟是一個輔助的器材,所以危險性也沒有到民眾擔憂的這麼大,「等身體一段時間癒合後就可以取出來,不過即便不取出來也沒關係,要看患者身體對其有無不適的反應,尤其這種鈦合金材質,不取出來其實無妨,民眾也不用過於擔憂。」
醫改會:「手術同意書」跟「自費同意書」規格應統一
至於要如何避免類似的事再發生?
醫改會研發組組長辜煜偉,接受《信傳媒》電訪時表示,第一步應從民眾的「手術同意書」跟「自費同意書」統一規格做起。「其實目前國內還沒有一個統一的規定,應該要把這個醫材的相關程序跟證號、相關標示都記載在自費的手術同意書上,讓民眾可以知道。」辜煜偉表示統一規格的重要性,在於資訊揭露也會給醫院壓力,院方必須去採購正確且符合衛福部食藥署的相關規範的合格醫材。
辜煜偉進一步表示,「其實衛福部食藥署有一個醫療器材的管理辦法,他們會依據醫療器材的風險等級分3級,每一級都有相關規範跟管理方式,他們也訂了醫療器材的優良製造規範,讓這些醫材廠商可以遵守,這個遵守其實要落實真的需要醫院跟政府端(包括食藥署跟衛福部)好好去做稽查或進一步追蹤,甚至提前去預防管理,而不是都裝進民眾身體裡才發現,我們覺得整個預防端都需要再加強。」
所以這次事件其實是食藥署明文條列都已規範出來,是院方執行上出現漏洞?
「我們如果講到母法,在台灣是依《藥事法》的規定去訂醫材的相關管理辦法,之前『台灣女人連線』常務理事黃淑英受訪時有表示,前2年台灣有要提醫療器材法的母法,但目前還躺在立法院。」辜煜偉指出,目前醫材的規範都還屬於子法甚至是行政指導的層次,還沒有像《藥事法》是屬於法律等級的法律,「如果政府能投入更多資源、也有一些對應的罰則跟管理規定,這樣廠商和醫院才能更嚴加地遵守。」
食藥署也提醒醫療院所,應持續關注使用該許可證產品的病人,若有疑似不良反應發生,應如實通報,並請有疑慮民眾可至原就診醫院詢問專業醫療人員。遲蘭慧也表示,食藥署將持續釐清產品回收狀況,若回收作業未確實執行,涉違反藥事法第80條,可處新台幣20至500萬元罰鍰。」