世界衛生組織在2020年3月11日宣布由新型冠狀病毒SARS-CoV-2所引起的傳染病COVID-19已經造成全球大流行(Pandemic)。截至2021年6月21日為止,已經有超過1億7千800萬人確診及超過380萬人死亡。
和所有其他傳染病一樣,宿主的免疫系統在對抗 SARS-CoV-2 感染的過程中扮演關鍵的角色,但免疫系統活化也會引起發炎反應,甚至造成嚴重的疾病。
WHO緊急批准AZ、BNT、莫德納、嬌生、科興、國藥6種疫苗
我們對宿主免疫反應的暸解有助於發展疾病的預防或治療的方法。免疫反應的組成,如抗體,也可用來開發具有靈敏性和專一性的診斷及治療的藥劑。雖然遏制和封鎖的手段可以暫時控制住,但我們終究需要有效的疫苗或治療的藥劑來阻止COVID-19的傳播與造成的傷害。
COVID-19疫苗的研發以前所未有的速度在進行,目前WHO緊急批准(Emergency Use Listing, EUL)的疫苗共有6種, 包含AZ (AstraZeneca)、輝瑞BNT (Pfizer-BioNTech)、莫德納 (Moderna)、嬌生 (Johnson & Johnson)、國藥 (Sinopharm)及科興 (Sinovac)。雖然世界各國在接種疫苗的人口比率各不相同,但是控制社區傳播的能力與疫苗接種率成正比。
台灣接種疫苗速度遠落後其他國家
由於台灣在全球大流行之前提早實施許多措施讓我們在去年及今年初只有少數感染案例。不幸的是,在最近幾個月,社區感染開始爆發了,並且讓疫情提升到第3級警戒。雖然政府有收購多種疫苗,而且台灣的疫苗公司所研發的疫苗也在進行臨床試驗,但台灣在接種疫苗速度卻遠遠落後於其他國家。
免疫學家在這場大流行中發揮了重要功能,包括開發診斷方法、治療試劑和疫苗。中華民國免疫學會 (CSI) 的會員也有積極的投入相關研究。另外,學會以 COVID-19 做為主題積極舉辦國內及國際的研討會,我們的會員也參與討論及分享有關台灣的疫苗公司所開發的疫苗及台灣的人民應該如何接種疫苗等議題。
近日國內因為COVID19疫苗相關議題,造成社會熱烈討論。中華民國免疫學會為結合臨床與基礎免疫學之專業學術法人,秉持學術單位的社會責任,以專業角度提供相關科學訊息。我們決定發布疫苗的相關公告,並向人民和政府提供建議。之後,我們還計劃定期發布常見問題的分析。其目的是希望總結事實、數據和實證的結論。
傳統與新型疫苗平台:發現新冠病毒兩個月後就發展出第一個RNA疫苗
新型冠狀病毒是單股有套膜的RNA病毒。在RNA遺傳物質外,這病毒還由核殼 (N)和包裹在病毒外的棘 (S)蛋白組成。這次疫情中,各家藥廠紛紛使用傳統與新型的疫苗平台-包含使用載體、DNA 和RNA,來製作抗新冠病毒的疫苗。
使用載體的疫苗可以經由插入病毒基因的抗原組成,在疫苗接種後可以體內產生病毒蛋白而引起具有保護性的免疫反應。其中,RNA疫苗是以可以在人體細胞內表達病毒蛋白的mRNA為主, 另外加以佐劑刺激免疫反應,並用特殊的包裹技術送入細胞內。
RNA疫苗可以很快速地在幾週內完全合成,並配製一定的數量足以做臨床試驗,這是在面臨潛在大流行時的一個寶貴的特色。這次疫情中,距離首次發現新冠病毒僅2個月就有第一個RNA的疫苗發展出來,並於2020年3月16日用於測試其在人類中的安全性。
傳統平台如去活化的新冠疫苗,則是利用體外的細胞株培養新冠病毒,並以化學的方式殺死病毒,達到去活化的效果。這樣的疫苗設計簡單快速,由於是包含整個病毒多個成分,會引發較複雜的免疫反應。
另外,蛋白質次單元的新冠疫苗,則是利用細胞株製造病毒的棘蛋白,再加上刺激免疫反應的佐劑。蛋白次單元疫苗中,作為抗原的棘蛋白的結構,還有佐劑的種類,對於誘發免疫反應的強弱非常重要。由於大量高純度蛋白質在開發與生產上比較困難,開發時間較長,製作成本也較高。
臨床試驗分為四期
臨床試驗是指將藥物用在人身上的研究,不同於細胞或動物實驗,這是驗證藥物有效性跟安全性的黃金標準。
第一期:是第一次將這個藥物用在人身上的研究,目的是探索藥物在人體上的安全劑量,還有潛在的毒性。針對疫苗的第一期(或是第一/二期)臨床試驗,主要評估疫苗在不同劑量安全性,並同時觀察免疫刺激的反應(如保護性抗體之產生)2,樣本數通常為數十人。
第二期:又稱為概念驗證(proof-of-concept)試驗,目的是初步有效性跟安全性的探索,通常是隨機雙盲對照式試驗,希望找出適當的有效且較少副作用的劑量。疫苗的第二期臨床試驗療效評估的指標通常是血中的中和性抗體,因為是雙盲試驗,解盲之後才知道受試者是使用試驗藥物或是安慰劑。樣本數通常是數百人到數千人。
第三期:又稱為確認性(confirmatory)臨床試驗。疫苗的第三期臨床試驗療效評估的指標是臨床感染率,重症率或死亡率等硬指標,這些硬指標的觀察,需要更長的時間以及更大的樣本數,因此樣本數通常是數萬人。
由於人體試驗時間較長,在現在新冠病毒疫苗臨床試驗中,會在施打疫苗後兩個月時執行期中分析,期滿完成通常需要兩年。大部分國家的藥物監管單位會在第三期臨床試驗期滿完成結果出來之後,根據實驗結果考察通過給予藥證。在目前新冠肺炎疫情的急迫性下,美國與歐盟採取評估第三期期中分析報告給予緊急授權使用(Emergency Use Authorization, EUA)。
第四期: 是藥物上市以後,使用在社區人群更大規模的上市後監測計劃,目的在評估長期的有效性及安全性。
疫苗保護力: 是指「接種疫苗的人群與沒有接種疫苗的人群相比,減少了多少罹病、重症或死亡的風險」。
疫苗效力(vaccine efficacy): 可經由嚴謹的臨床試驗得知,然而每個臨床試驗的研究方法、執行地點與評估指標均不相同,所以不建議直接比較不同疫苗的臨床試驗結果,並以此評斷疫苗的優劣。
全球開發中的新型疫苗共287款,至少102款已進入臨床階段
根據WHO數據,截至110年6月18日,全球開發中的新型冠狀病毒疫苗共287款,其中至少102款已進入臨床試驗階段,23款進入第三/四期臨床試驗,14款在不同國家獲緊急授權使用。下面的資料謹簡要的提供世界上用的最廣泛的三個疫苗:
輝瑞BNT:
種類: RNA
收案人數*: 43,548
疫苗保護力**: 95%
莫德納:
種類: RNA
收案人數*: 30,420
疫苗保護力**: 94.5%
AZ:
種類: 腺病毒載體
收案人數*: 23,848
疫苗保護力**: 81.3%
(*: 第三期臨床試驗; **評估項目: 降低確診人數)
台灣的國產疫苗近况
高端疫苗(次單位疫苗)
第二期臨床試驗共計有3,815名受試者完成第二劑疫苗施打(65歲以上838人)。在6/10日公布的二期期中結果解盲,顯示疫苗有高的安全性,中和抗體: 不分年齡疫苗組的血清陽轉率為99.8%,其中20至64歲疫苗組族群為99.9%4。
聯亞生技(次單位疫苗)
第二期臨床試驗共計有3,844名受試者完成第二劑疫苗施打 (65歲以上792人)。預計將在六月下旬公布二期期中結果。
WHO估算至少7成人打疫苗 COVID-19疫情才會結束。下圖為世界幾個國家施打疫苗的情况。
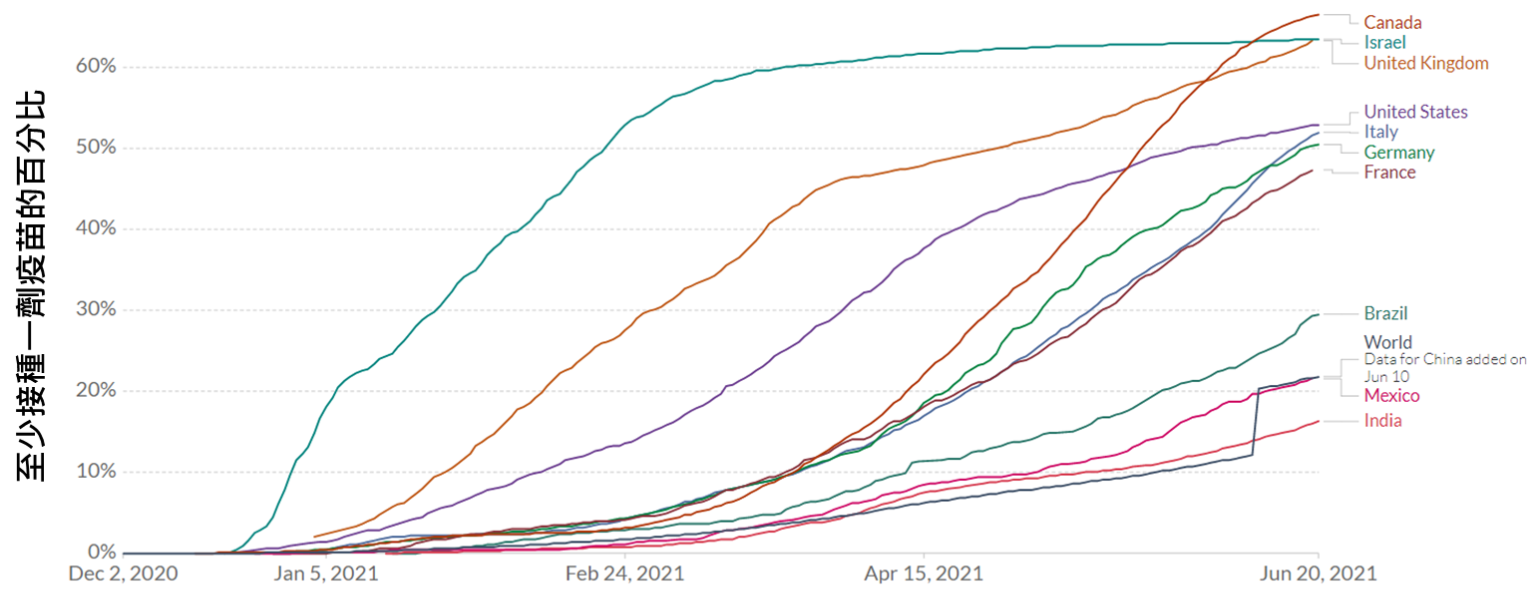
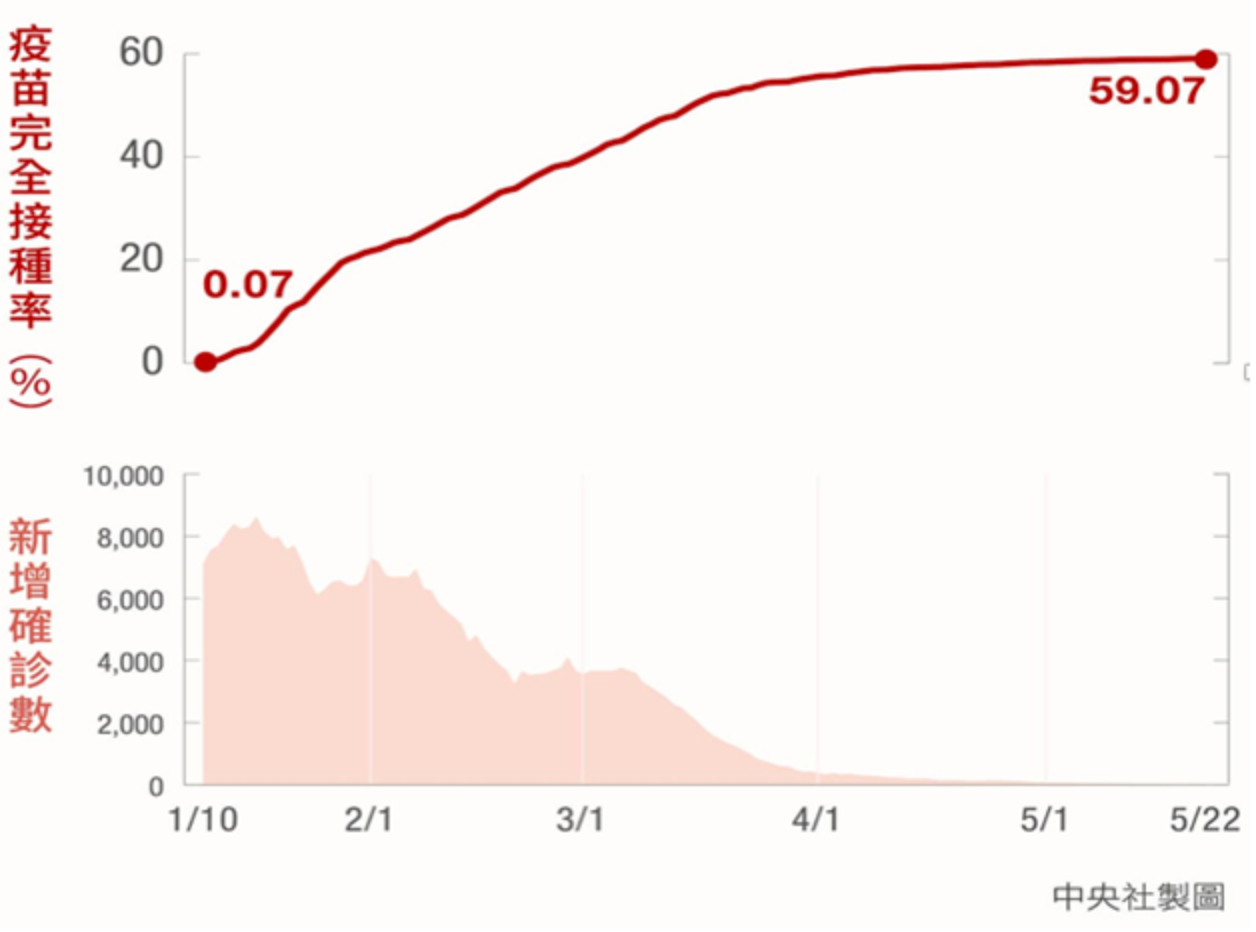
全球疫苗接種率第二高國家:以色列重症比例減少92%
以色列人民自2020年12月起就接種輝瑞BNT疫苗,是截至2021年6月全球少數幾個已達成「群體免疫」的國家之一,打完2劑疫苗接種率近6成 (目前全球疫苗接種率第二高的國家)。因有效疫苗的接種,使得以色列的新冠確診數持續下滑 (下圖),由2021年1月單日確診數超過1萬例,才短短3個月(2021年4月)就降到130例。直到2021年6月,單日確診數皆在兩位數以下。
根據官方數據及國際期刊分析結果,自疫苗開打以來,以色列的新冠感染率、住院率、重症率和死亡率都顯著降低。以色列最大的健保機構『大眾健康服務(Clalit Health Services)』,近期針對疫苗保護效力進行比對研究,結果發現60萬名完成兩劑疫苗者,比起60萬名未接種疫苗者,有徵狀的確診比例下降94%,重症比例也減少92%。
與此同時,以色列境內也邁向全面解封,越來越多人前往公共場所活動,回歸正常生活。由此可見有效疫苗的接種對於新冠感染率與重症率和死亡率都有顯著的效應。
台灣採購疫苗進度及接種及接種人次
疫苗採購數量 (資料截至06/21/2021): COVAX: 476萬劑;AZ: 1,000萬劑;莫德納: 505萬劑;國產疫苗: 高端: 500萬劑;聯亞: 500萬劑;累計採購2,981萬劑。剛好達到台灣居民的群體免疫(一個國家或地區至少60%的人口比例應該完整接種兩劑疫苗或產生抗體)的需求,但是目前尚未全部到貨並施打。
另外,日本捐贈約124萬劑AZ疫苗及美國捐贈250萬劑莫德納疫苗,累計總到貨量只有約485萬劑。截至6月21日,國內累計接種疫苗有 1,541,732人次。其中接種AZ疫苗有 1,478,402人次, 莫德納疫苗有 63,330人次。
免疫橋接仍待學界與各國法規討論達到共識
1、SARS-CoV-2疫苗研發緊急,各種技術的疫苗已經緊急上市或是開發中。國產疫苗採用的是蛋白質次單元疫苗,技術較為穩定成熟,學理上安全性比較理想。然而人體,疫苗與病毒間的交互反應非常複雜,沒有足夠的科學與臨床研究報告出來之前,安全性與有效性無法定論。
2、臨床試驗是非常專業的學問。第二期主要是初步探討有效性,而第三期則是大規模驗證有效性與安全性。目的不相同,實驗設計也會有不同。目前幾個主要緊急核准的疫苗,包括AZ,輝瑞,莫德納疫苗,都是在做了第二/三期或第三期試驗後,利用初步的結果直接申請緊急使用。
3、國產疫苗目前在第二期人體試驗的誘發抗體反應的評估,是用受試者因疫苗產生抗體的濃度,以及在體外實驗中的中和病毒感染能力當作指標。
4、目前各國疫苗需求孔急,加上科學研究的進展與實際執行三期研究的困難。WHO與各國廠商已開始討論是否可以放寬用所謂免疫橋接(Immune bridging study),也就是用體外免疫學實驗來驗證保護力,作為申請緊急使用的標準。目前學界的研究,也認為體外免疫學研究和臨床保護力之間有明顯關聯性。這點仍待學界與各國法規討論達到共識。期望政府與國產疫苗廠商,能跟上世界規範變化,加速疫苗的開發,造福國人。
5、製藥是一個結合商業,科學,醫學與政府法規的複雜活動。需要各方專業人士的參與合作,並受到學術,醫學倫理與法規的嚴格規範。由於疫情孔急,美國與歐洲政府,因應疫情給與大量的行政上的方便與加速的協助。在科學為基礎上也大幅簡化相關要求與規定,並根據規定執行獨立與超然的審查。除了在緊急情況下,盡力保證人民的安全,也得到各國政府與人民的信任。
6、政府為疫苗與藥物審查單位,需要超然立場。政府相關人員不應該對疫苗研究與效果做非正式的發言,違反行政中立。疫苗臨床研究成果,應統一由該公司按照學術倫理與政府規範統一發布正式新聞。
7、科學是解決疫情唯一的方式。在這人心最不安的時候,更需要拋開個人的意見與立場,以數據與科學作為依據,做出正確的決定。
科學與疫苗將幫助人類走出這次世界危機。在此同時,台灣2300萬人同島一命,請大家互相理解合作,相信科學,帶台灣盡快走出這次危機。免疫學會也將秉持專業,提供社會正確的科學資訊。
參考資料
Sadoff et al. N Engl J Med 2021; Walsh et al. N Engl J Med 2020
https://www.who.int/publications/m/item/draft-landscape-of-covid-19-candidate-vaccines
https://www.medigenvac.com/public/news/detail/78?from_sort=1
https://ourworldindata.org/covid-vaccinations
N Engl J Med 2021; 384:1412-1423