幾十萬人打的疫苗,花了納稅人幾十億。身為醫生不寫監督高端疫苗的文章,要寫什麼?
新冠次蛋白疫苗,發展初期學界就認定開發時程太長,有製程Scale Up放大的困難,不適合大流行。果然,次蛋白疫苗領頭羊Novavax因為量產問題卡關,無法通過美國EUA而一直延遲上市。台灣高端疫苗,雖然開打了,但產能問題看來同樣難以突破。
CDE要求產能標準不同:高端50升vs.聯亞2000升
次蛋白疫苗,是以細胞培養製造蛋白質抗原(見附圖下)從小的反應槽開始,培養細胞增殖後,要不斷的換容器,一直換到2,000升的生物反應槽,大量的細胞成為生物工廠,才能有夠大夠快的產能。
但是,要保持產品的穩定性,更換到較大容量的反應槽是技術上的門檻。每次收獲完一批蛋白質後,大量細胞就沒用了,又要從頭開始培養。高端疫苗到最新公佈通過的一批批號,仍然無法Scale UP,還停留在50升低階製程上。
聯亞新冠疫苗雖然沒有通過EUA,但他們的創辦人王長怡博士在記者會上講過,台灣CDE(財團法人醫藥品查驗中心)要求聯亞以國際通用的2,000升製程做臨床實驗,並成為上市後的製程標準。但最近聯亞才發現,高端竟然是以2升的製程做實驗,以50升的製程來生產,聯亞高層集體抓狂,表示無法置信。
一個生物反應槽生產出來的抗原蛋白是一個批次,高端疫苗總共送食藥署檢驗的有22個批次,其中有3個批次是2公升製程,食藥署採用其中1個批次。有4個批次是200公升製程,但全部失敗無法通過檢驗。其餘工廠送出來15批50公升製程的批次中,只有11個批次通過食藥署的檢驗,通過率是73.3%。
最新(9/7)通過一批的批號是SP2122(推估出廠日7/23),還是50升製程,前一批通過的是SP2120(7/16出廠50升製程),也就是說中間的SP2121那一桶的產品沒有通過,食藥署未說明原因。
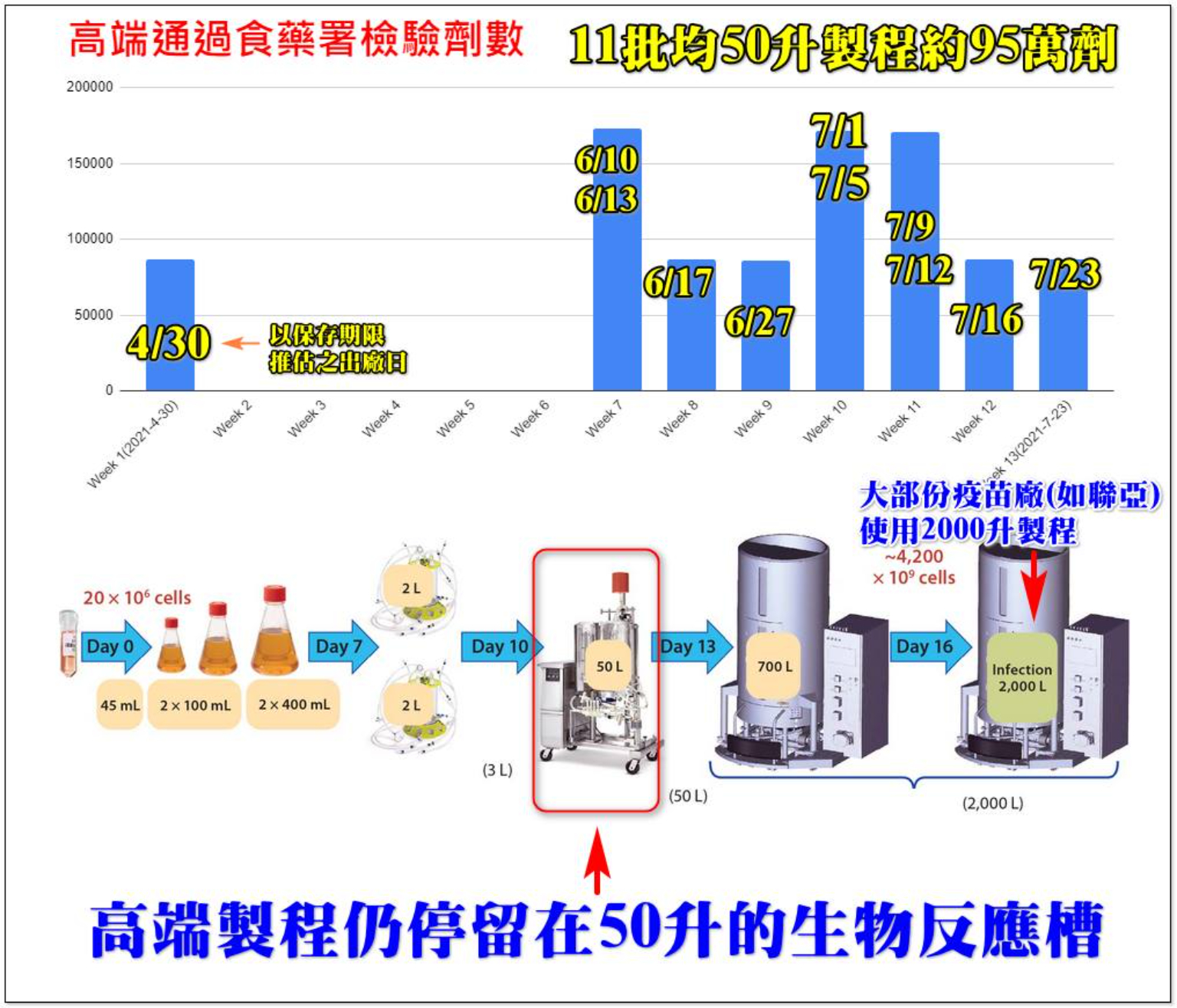
高端這11批的50升製程疫苗,總共95萬劑,是高端從4月底到7月底的總產能,生產完之後,食藥署檢驗封箴高端一批貨要花1.5個月。計算生產速度,高端最高紀錄是一個星期,只能生產出18萬劑的疫苗(見附圖上)。
高端產量、良率皆低,年底前最多再生產288萬劑
下一波高端接種,9/28號開打。之前打過第一劑的71萬人,已經28天了,要打第二劑,現在庫存的疫苗約24萬劑,就算沒有人新打第一劑,要打完所有的第2劑,也還欠了47萬劑差額。食藥署在8/1的新聞中承認,整體收到的高端疫苗數不超過百萬劑。現在只剩兩個星期,這47萬劑疫苗要能如期生產出來,並通過食藥署檢查有點勉強,要靠運氣。
預估到年底,只剩3.5個月,16個星期,以最高速每星期18萬劑來算,16x18=288,等於288萬劑,這還沒扣掉食藥署約6個星期的檢驗封箴時間。生產速度如果沒有提昇,製程沒有放大,怎麼可能到年底前再生產出400萬劑,而達到政府設定今年500萬劑的目標?
這裏就先不談高端沒做三期臨床實驗,保護力不明了。高端光是產能有限,良率太低,連國內的需求都無法及時應付,就是致命的缺點,以美國國產Novavax疫苗的標準來看,產能不夠力,在美國是不會通過EUA的。病毒不等人,台灣下波疫情隨時可能爆發,人民沒有時間慢慢等待高端把製程優化。
新冠病毒變種的速度,快過次蛋白疫苗製程放大需要的時間
新冠病毒變種的速度,快過次蛋白疫苗製程放大需要的漫長時間,等到製程優化完成,病毒早已不是原先用的基因序列。這也是歐美花費巨資投入能快速生產的mRNA疫苗的主因。
國際疫苗常常飛來一個航班,送到的劑量就比高端3個月來的總產量還高。郭董BNT疫苗不給高端面子,不講武德,2個月前才買到的1,500萬劑,現在能保証其中的800萬劑,分批送貨的飛機周周都會到。
政府快點醒醒,別再固執,原先規劃的2,000萬劑國產疫苗中,1,000萬劑是聯亞,EUA沒過,另外1,000萬劑是高端,產能不行加保護力不明,2,000萬劑的配額空在那裏變成防疫的大破口。國產疫苗產業遠遠沒有國人生命健康重要,疫苗廠那一點營業額連半導體產業的零頭都不到,需要趕快改變戰略,以千萬劑為單位,再加購國際疫苗,買的越多貨才會到的越快。
COVAX擺爛,現在政府直接向廠商買AZ加莫德納1,505萬劑是絕對不夠的,訂貨數量遠低於其它國家的情況下(如波蘭三千七百萬人口訂了一億劑),要催貨也催不動。
台灣打到第二劑疫苗的人不到5%,我3個月前就打過第2劑AZ了,一直以來,我是在為你和你的家人朋友,爭取打到疫苗保障生命的機會,這是醫生的天職,對社會的責任。一篇文章不夠,那我就寫十篇一百篇,繼續努力,你也可以一起出力。
本文轉載自潘建志臉書