根據1997年聯合國糧食及農業組織╱世界衛生組織所定義的,膳食中的碳水化合物依分子的聚合程度(degree of polymerization, DP)分為三大類:糖(DP 1-2)、低聚醣(短鏈碳水化合物,DP 3-9)和多醣(DP 10)。 我們會聽到有很多複雜的稱呼,例如:單糖和雙糖、多元醇、低聚醣、澱粉、修飾澱粉、非澱粉多醣等。雖然碳水化合物的作用跟主要化學成分有關,但物理性質都會發生改變,例如:水溶性、水合作用、凝膠形態、結晶形成、與其他分子(例如:蛋白質、脂質和二價陽離子)的結合,以及存在細胞壁和其他特殊植物組織中聚集成的複雜結構。
本章的重點放在不同碳水化合物的營養作用和生理特性對健康的影響。
適當的難消化碳水化合物對人類健康非常重要
在攝入澱粉食物後,經過唾液澱粉酶、胰澱粉酶後的澱粉類由多醣變成雙糖,在小腸變成單糖形式(葡萄糖、果糖和半乳糖)後,均在空腸近端被吸收進入絨毛內的微血管,再經由門脈系統進入肝臟,然後循環至全身細胞利用。其在小腸上皮細胞吸收的方式有:(1)葡萄糖與半乳糖以共同運輸的方式進入上皮細胞內,(2)果糖以促進性擴散的方式進入上皮細胞內。除了上述可消化的單糖,剩下不可消化、可以直達大腸的碳水化合物(膳食纖維,或是某些特殊糖),會被大腸內的細菌發酵後,產生一些有益的代謝產物。若碳水化合物不足,腸道菌會轉向其他的替代能源,導致產生對人體有害的代謝產物,所以適當的難消化碳水化合物對人類健康來說非常重要。
膳食纖維是人體無法消化的多醣,又被稱為MACs(microbiota-accessible carbohydrates, MACs),就是指「腸道菌可利用碳水化合物」,它們的性質就是「不會被人體消化酶所分解吸收的植物剩餘物」,是對人體能產生益處的不可消化的碳水化合物,也是腸道菌群的主要能量來源。飲食中MACs 的豐富度及多樣性可調節腸道菌群組成及功能,從而影響宿主免疫及健康。在研究中發現,缺乏MACs 的飲食(例如:西式飲食)會破壞腸道的平衡,惡化了發炎性相關疾病的發展,包括過敏性疾病、感染、自體免疫疾病等等。某些可消化的多醣類仍然被歸類為膳食纖維,是因為當它們混在食物當中時,消化酶無法輕易到達分解,例如:第一型抗性澱粉。膳食纖維根據水溶性、黏度、結腸中的微生物發酵程度,以及刺激某些細菌生長的能力等標準,分為三大類:
❶ 可溶性膳食纖維 ( Soluble dietary fiber, SDF )
非纖維素多醣 (non-cellulosic polysaccharides)、寡糖(oligosaccharides)和親水膠體(如果膠pectin)、β- 葡聚糖(β-glucan)和樹膠
❷ 非可溶性膳食纖維( Insoluble dietary fiber, IDF )
纖維素(cellulose)、半纖維素(hemicellulose)、木質素(lignin)、抗性澱粉 (resistant starch)和梅勒氏反應產物(Maillard reactions)。
❹ 益生元膳食纖維 ( Prebiotic dietary fiber ):
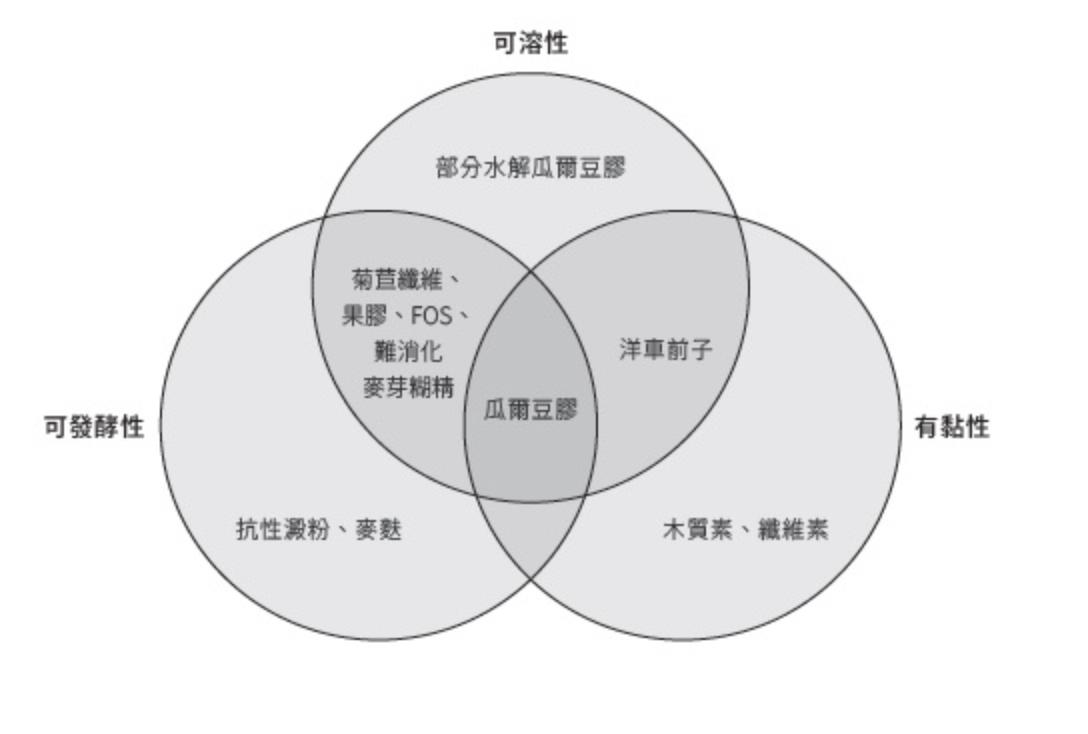
菊苣纖維(inulin)、菊粉型果聚糖 (inulin-type fructans)、反式乳寡糖(trans-galactooligosaccharides)和果寡糖(fructooligosaccharides, FOS)、L- 阿拉伯糖也屬於此類。這類短鏈的碳水化合物有利於雙歧桿菌的增加,但也可能因產生太多氣體而造成腹脹問題。另外,有些是同時具有水溶性、黏性、發酵性的其中幾中重疊分類,示意圖如下:
研究發現,長期缺乏MACs 的飲食會讓腸道的微生物多樣性越來越差,而且有代代相傳的趨勢。這些好菌數量降低的貧瘠菌相到了第三代後,即使再補充纖維也無法恢復原貌。
非水溶性纖維(如燕麥纖維有2/3 的非水溶性)的主要功用可增加糞便體積、幫助排便,減少有害致癌物質在腸道的時間;而水溶性纖維(如菊苣纖維)可吸附毒素、減緩醣類跟脂肪吸收,且為腸道益生菌的營養來源,可被細菌分解利用。2016年發表於期刊《Cell》上的研究更顯示,
膳食纖維攝取不足,腸道內的細菌就容易分解腸壁黏膜細胞層,導致病原菌及毒素進到血液。故同時攝取足量兩種纖維有助於減少大腸癌及疾病的發生,維持腸道益菌的生態平衡。
每個MAC都具有其獨特的特性
這些可越過胃跟小腸直達大腸的MAC,可以經腸道細菌的作用下,產生一個對人體健康很重要的產物──短鏈脂肪酸(Short-chain fatty acids,以下簡稱SCFAs),包括丁酸(butyrate)(15%)、乙酸(acetate)(60%)和丙酸(25%)。舉例來說,乙酸和丙酸跟肝臟中代謝脂質,葡萄糖和膽固醇有關,前者是膽固醇合成和脂肪形成的前驅物,後者是糖質新生的基質。而丁酸在維持組織屏障功能,以及調節基因表達和免疫調節中扮演至關重要的角色。SCFAs 能穩定腸道、刺激上皮細胞的增殖和分化、鹽和水的吸收、維持黏膜完整性並減少炎症。此外,SCFAs 還瘦體素,還有對抗肥胖。
每個MAC都具有其獨特的特性,未來可以作為精確的腸道微生物群調節劑,來促進宿主的腸道穩態。這在後面精準營養食代來臨的章節會再詳細介紹。但即使是抗性澱粉這類在傳統被認為有利健康的碳水化合物,依照每個人的腸道菌相和基因不同,也可能會有截然不同的結果。
譬如說,每個人腸道內擬桿菌門(Bacteroidetes)當中占比最多的兩個菌屬:善於利用碳水的「普雷沃氏菌屬」(Prevotella)和善於利用蛋白質「擬桿菌屬」(Bacteroides)的比例(P/B ratio),會影響到特定碳水飲食的減重效果。
未必每個人都是吃高纖澱粉的減重效果較好
在哥本哈根大學的研究者Mads Fiil Hjorth 一連針對腸道的P/B ratio,在不同期刊發表了三篇研究 。起因在依照丹麥國家建議的飲食標準,多攝取水果、蔬菜、高纖和全穀類(富含抗性澱粉)食品,也只有「約一半」的人能達到減重效果,其餘一半人口並無法從中獲得減重成效。
所以他在起始點把肥胖受試分成「高P/B 比」跟「低P/B 比」的兩族群。
分別介入新北歐飲食(NND)跟傳統丹麥飲食(ADD),前者比後者更高纖、高蛋白質跟低脂,以全穀類等高纖維澱粉為主食。
第一篇結果發表在《國際肥胖雜誌》(International Journal of Obesity)28,研結果顯示只有「高P/B 比」的人,使用NND 飲食的效果會明顯好於
ADD(-4.5kg vs -1.09kg,有顯著意義差距)。若是起始菌相「低P/B 比」的人,吃NDD或ADD的差異不大(-3.27kg vs -2.11kg)。而且看起來,傳統丹麥飲食用在「低P/B 比」的人身上,比用在「高P/B」的人效果更好。意即未必每個人都是吃高纖澱粉的減重效果較好。後來他在2019年做第二篇復胖的研究,發現這些「高P/B 比」的人,在吃低纖維高脂肪的「西式飲食」,復胖的體重遠遠超過「低P/B 比」的人。我推測是西式飲食低纖維高脂肪,讓大腸的普雷沃氏菌(Prevotella)沒食物可利用,有點類似根莖類食物造就非洲原住民的菌相,也是以普雷沃氏菌(Prevotella)為主,若移民到西方吃低纖維飲食會快速變胖的原因。
第三篇2020年加入一個人類基因「AMY1 CN」跟飲食,還有腸道菌的互動研究,這個基因和唾液澱粉酶的表現有關。越高的人對於澱粉的消化吸收能力更好。研究發現,在「高澱粉酶基因」的受試者中,吃NDD 或ADD 飲食在高或低P/B 比的減重效果都沒有差異。而「低澱粉酶基因」的人身上,吃這兩種飲食會依據P/B 比的高低, 而有不同的結果。有這樣的差異原因,猜測是「高澱粉酶」的人對澱粉的分解能力極佳,從口腔到小腸就變成小分子吸收,能夠到達大腸給腸道菌作用的不多;而低澱粉酶的人因為澱粉的消化不好,更容易讓高纖維碳水來到大腸,讓普雷沃氏菌(Prevotella)作用,產生較多短鏈脂肪酸,而有較好的減重效果。
另外也能猜測,之所以吃完「高脂肪極低碳飲食」的人,一吃澱粉就復胖快速,可能跟身體的碳水來源不足。所以AMY基因上調,或是小腸當中協助利用碳水的菌代償性增加,讓碳水食物都能有效被分解利用,能藉由表觀遺傳調控(epigenetic regulation)來抵抗癌症,並且能刺激許多跟飽足感有關的激素分泌(例如:glucagon-like peptide、 peptide YY、因此一吃高碳飲食就加倍吸收有關。
由這三個飲食研究可知,光是人類的澱粉酶基因高低× 高or 低纖維飲食× 高or 低P/B ratio,就有8種組合,但只有一種人(低澱粉酶&高P/B ratio)可以從高纖維澱粉的飲食中得到減重的好處。因此關於碳水化合物的攝取,除了以高纖維跟腸道菌可利用為大方向,但還是要依每個人的狀況不同,而找出適合的食用方式,包括有些容易脹氣的人或是易腹瀉的人,在含纖維的碳水攝取上可能就要有所限制。相關的碳水攝取注意事項,會在各疾病章節再詳細介紹。